見て,操作して,知る,そして,役立てる
細胞型試験管:セミインタクト細胞
生体分子の機能発現やその制御メカニズムを試験管内だけで研究し議論することが限界になってきています.何故なら,例えば,タンパク質は,細胞内の特定の場所(空間)で特定のタイミング(時間)でその機能を最大限に発揮するよう進化してきたため,「真の」機能やその制御メカニズムの研究にはタンパク質が機能する「環境」を考慮した実験システムが必要不可欠だからです.特に,オルガネラや細胞骨格が作る細胞固有のトポロジー「空間」をどの様に実験系に導入し解析するかが重要なことになってきています.例えば,神経細胞の樹状突起や成長円錐など特定の場所へと生体分子を選別して集積させる細胞内物質輸送・ターゲティング機能の研究は,細胞をすりつぶして行う従来の生化学的手法のみに依存した実験系では困難です.何とかして,生体分子が機能する「空間」情報と「時間」情報を考慮に入れた環境でタンパク質やRNA/DNAの機能解析を行いたい.セミインタクト細胞は,このように「細胞内での」生体分子の機能解析を扱う最新の生命科学の要請から生まれてきた「細胞型試験管」です.
セミインタクト細胞とは細菌毒素などを用い細胞膜を部分的に透過性にした細胞のことです1) 2).細胞内の様々なオルガネラや細胞骨格(アクチンフィラメントや微小管など)のトポロジーを保持したまま,細胞質を細胞外へ流出させた細胞です.細胞を一個の試験管に見立てて,ここに新たに外部より調製した細胞質成分やタンパク質,エネルギー源であるATP再生系などを戻してやると,添加した細胞質に依存的な生命現象を「再構成」することができます.再構成できれば,加えた細胞質成分の中のどんな因子が,どのようなメカニズムで生命現象に関わるか・制御するかなどを生物物理学的・生化学的手法を使って解析できるというわけです(図1).例えば,正常な細胞をセミインタクト細胞にして,ある病態を示す細胞・組織から調製した病態細胞質を添加してやれば,「病態モデル細胞」ができるため病態細胞と正常細胞内で生起する生命現象を分析的に再構成し比較解析することができるのです.私の研究室ではこの“マニアック”な細胞実験系とイメージング技術をカップルさせた世界に類を見ない「セミインタクト細胞アッセイ」を多数作り,様々な生命現象の解析に応用しています.
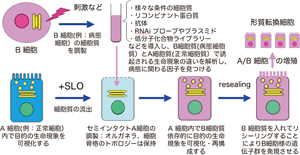 図1 セミインタクト細胞アッセイ自動化装置を中心とした細胞チップ自動可視化システム
図1 セミインタクト細胞アッセイ自動化装置を中心とした細胞チップ自動可視化システムセミインタクト細胞アッセイの例:Organelle architectonics(図2参照)
細胞分裂(M期)の際,遺伝情報をおさめた染色体や細胞質が分配されるだけではなく,細胞の諸機能を司るオルガネラもふたつの細胞に正確に分配されねばなりません.特に,シングルコピーで存在するゴルジ体,小胞体(間期の小胞体は,チューブ状の膜が三つ叉構造を基本単位として連なった単一のネットワーク構造をとる)の分配制御機構はオルガネラ発生学における謎の一つでした.
「見る」:私たちは,先ず,GFP可視化法によりゴルジ体と小胞体の分配過程のリアルタイム可視化を行い,間期とM期のゴルジ体と小胞体の典型的な形態を明らかにしました.間期のゴルジ体は核の一極に集まるリボン状構造体ですが,M期では,一旦大まかな構造体(mini stack Golgi)に分解し,続いて細胞質中により小さな膜小胞として分散します.そして,娘細胞に確率論的に分配され再びシングルコピーのゴルジ体となります.間期においてネットワーク構造を持つ小胞体は,M期になっても小胞化しません.むしろ,ネットワークの一部が部分的に切断された状態で,小ネットワークに固まりとして娘細胞に分配され再び連結して大きなネットワーク構造を作ります.
「操作して,知る」:ゴルジ体や小胞体ネットワークをGFP可視化した細胞株を樹立し,それからセミインタクト細胞を調製します.そこにM期の細胞質を導入してM期のゴルジ体や小胞体ネットワーク構造を再構成しました.さらに,M期の細胞質を洗い流しそこに間期細胞質を入れて間期のゴルジ体・小胞体ネットワークを再構成できました.また,間期・M期細胞質を生化学的に分析し,部分的に切断されたM期の小胞体ネットワークや小胞化したゴルジ体膜を間期のものに戻すには,細胞質中の「NSF/SNAPタンパク質複合体」と「p97/p47/VCIP135タンパク質複合体」がゴルジ体膜や小胞体膜の膜融合を誘起していることや,M期に活性化するcdc2 kinaseがp47をリン酸化することにより「p97/p47複合体」が失活してM期の小胞体の部分的切断やゴルジ体の小胞化が起こることも明らかにしました.面白いことに,M期におけるゴルジ体の分解にはcdc2 kinaseの前にMAP kinase kinase(MEK1)が必要であること,小胞体ネットワークの再構築には上記のタンパク質複合体が「順番に機能して」小胞体ネットワークを再構築させますが,ゴルジ体の場合は,2種類の複合体が「並行して機能する」点が違うことも判りました.
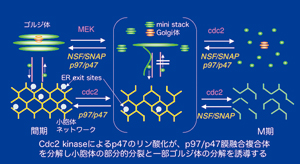 図2 細胞周期依存的なゴルジ体・小胞体ネットワークのオルガネラ創成機構と小胞輸送とのカップリング(解説:本文参照)
図2 細胞周期依存的なゴルジ体・小胞体ネットワークのオルガネラ創成機構と小胞輸送とのカップリング(解説:本文参照)小胞体とゴルジ体は,独立したオルガネラであると同時に両方向性の小胞輸送によって結ばれています.われわれは,セミインタクト細胞とGFPのフォトブリーチング法を用いて小胞体?ゴルジ体間輸送も可視化再構成しました.この様な2つのオルガネラ間の小胞輸送アッセイにはオルガネラの空間配置とオルガネラを結ぶ細胞骨格(微小管)が作るトポロジー保持状態の実験系が必要不可欠ですので,セミインタクト細胞アッセイは最適なのです.実験の結果,M期においてのみ,小胞体→ゴルジ体の順行輸送がcdc2 kinase 依存的に停止することが判りました.ER膜上には,ER exit sitesというリボソームフリーの膜ドメインがあり,ここは,ゴルジ体へ輸送されるタンパク質が輸送小胞(COPII小胞という)に積み込まれる特殊な膜ドメインです.実は,この膜ドメイン形成にp97/p47タンパク質複合体が関与し,cdc2 kinase依存的なp47のリン酸化によってそのER exit sitesが分解し順行輸送過程のみを選択的に止めたのです.
この様に,セミインタクト細胞アッセイを駆使した解析結果と最新の情報を総合的に解析すると,小胞体,ゴルジ体の形態形成制御機構(Organelle architectonics)及び両オルガネラ間の小胞輸送がcdc2 kinase依存的なp97/p47の膜融合装置のリン酸化を中心としたタンパク質ネットワークにより実に巧妙に制御されていることがわかりました.
始動するセミインタクト細胞技術
上の例でも判るように,セミインタクト細胞アッセイ系は複雑で協奏的に起こる生命現象を,形態学的に生化学的に素過程に分割し,それぞれの素過程を制御するタンパク質や脂質や核酸の機能を解析・検定できることが特長です.2007年度には,3年の月日をかけた「セミインタクト細胞チップ」と「セミインタクト細胞アッセイ自動化装置」そして,「チップ自動可視化システム」が相次いで完成しました(図3).これらシステムの導入により,セミインタクト細胞アッセイのハイスループット化が可能となり,アッセイを基礎生物学的課題に利用できるだけでなく,細胞を利用した薬物スクリーニングや病態診断システムなど創薬・診断支援システムとしても応用が期待できます.
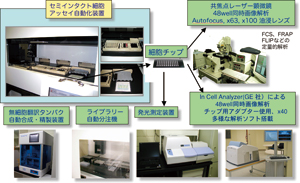 図3 セミインタクト細胞を用いた生命現象の可視化・再構成とリシーリング技術を利用した細胞工学的応用のスキーム
図3 セミインタクト細胞を用いた生命現象の可視化・再構成とリシーリング技術を利用した細胞工学的応用のスキーム最後に,セミインタクト細胞技術を用いた夢のようなプロジェクトが始まりました.それは,ヒトやマウスの体細胞のセミインタクト細胞にES細胞の細胞質や特定のタンパク質群を導入してからリシーリングし,核内のDNA情報をエピジェネティックに改変し誘導型多能性幹細胞(iPS細胞)を作成する試みです.これができれば,核移植・細胞融合やウイルスを用いない全く新しいiPS細胞ができることになり再生医療に大いに「役立てる」ことができます.又,セミインタクト細胞内に標識したタンパク質を導入してからリシーリングし,細胞内での生のタンパク質構造を構造生物学的手法で解析するプロジェクトも開始されました.これが成功すれば,細胞内の機能するタンパク質の構造を初めて「見て,操作して,知る」ことができます.いろいろな人が,いろいろな技術とカップルさせ成長させ利用していけるのがセミインタクト細胞アッセイの真骨頂です.