酸素原子と水素原子からなる
新しい不安定分子と分子錯体の検出
はじめに
我々の研究室では,通常の条件下では反応性が高く,単離して詳細に調べることの困難な分子種を気相の高分解能分光の手法を用いて検出し,その詳細を調べている.用いている実験手法は,気相分子の回転状態の変化をマイクロ波により検出するマイクロ波分光法や,分子内の電子状態の変化に伴う電子遷移をレーザーを用いて観測するレーザー分光法などである.反応性の高い分子を効率的に生成し観測するためには,数十センチメートル径の真空槽中に分子を超音速ビームとして吹き出す手法を用いている.実際に我々の装置で観測対象となるのは,数原子程度の比較的簡単な分子種であるが,電波天文学で宇宙空間中に発見される分子や,大気化学で重要な反応中間体には,反応性の高い未知の分子が数多く存在しており,我々の装置ではそのような分子の研究を積極的に行っている.本稿では,最近我々の研究室で検出した酸素と水素原子のみからなる非常に簡単ではあるが,ほとんど未知の新しい分子種の検出を紹介する.
不安定分子,フリーラジカル,ラジカル錯体
紹介するのは,最近我々がマイクロ波分光法で検出したHO3,HO3H,H2O-HO2の3つの分子種である.これらはそれぞれ3つの酸素原子を含み,水素原子を1から3個含んでいるが,それぞれ異なる性格を持つ.最初の分子,HO3は不対電子を持つフリーラジカル(日本語では遊離基と呼ばれる)である.不対電子を持つため本質的に反応性に富んでおり,単離することはまず不可能である.これに対し,HO3Hは不対電子を持たない閉殻の分子である.そのため,必ずしも反応性が高いとは限らず単離できる可能性もある.実際,極低温の溶液中に存在するという報告もなされているが,孤立した分子として安定に取り出しうるかは不明である.我々は,超音速ビーム法を用いているため,反応性の高いこれらの分子も,特に制約なく検出可能である.最後の分子,H2O-HO2は,分子式の示すとおり,孤立した一つの分子ではなく,水分子H2OとHO2ラジカルとが弱い分子間力で結合したラジカル錯体と呼ばれているものである.HO2ラジカルは,大気化学で重要な役割を果たしている反応中間体ラジカルであり,その振る舞いの解明は大気化学を理解する上で非常に重要である.最近,このラジカルが大気中に存在する他の分子と弱い分子間力で結合することにより,その反応性に様々な影響が見られるのではないかということが議論されている.特に水分子との錯体には,大きな注目が集まっていた.我々の研究は,この錯体を初めて検出したものである.
生成と検出
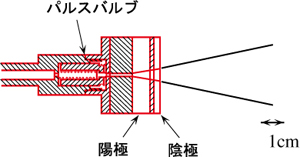 図1 パルス放電ノズルの概念図.図の左側がパルスバルブで,その先端に付けた陽極と陰極の間に1000〜2000 Vの高圧パルス電圧を掛けて試料気体を放電する.放電生成物が,超音速ビームとして右方向に放出される.
図1 パルス放電ノズルの概念図.図の左側がパルスバルブで,その先端に付けた陽極と陰極の間に1000〜2000 Vの高圧パルス電圧を掛けて試料気体を放電する.放電生成物が,超音速ビームとして右方向に放出される.これらの不安定分子は,上でも述べたように大きな真空槽中に超音速ビームとして分子を流し,その中に存在する分子をマイクロ波の吸収で検出するという方法で研究する.目的の分子は,図1に示すようなパルス放電バルブを用いて生成した.超音速ビーム法は真空中に約0.8 mmの孔から分子を急速に噴出することにより,分子が断熱膨張を起こし,内部温度が数K程度まで低下するとともに,進行方向のそろったビームとなることを利用する.真空ポンプに過大な負担を掛けないで質の良いビームを生成するために,パルス的に分子を噴出する.これに利用するパルスバルブの先端に電極を装着し,その中でパルス放電を行う.上記の3種の分子ともほぼ同様の生成条件で生成することができた.即ち,アルゴン中に10%程度酸素を混ぜた混合気体を作っておき,それを水または過酸化水素水の上を通し,少量の水,あるいは過酸化水素を含んだ気体とし,それを放電するのである.
しかしながら,ほぼ同様の生成条件で生成するということは,裏を返せばこれらの分子種が同時に混ざり合って観測されるということである.幸いにもマイクロ波分光法は分解能が非常に高いので,多くの分子種の混合気体から目的の分子の信号だけを取り出すことができる.しかし,数多く観測される信号から,どれが目的の分子のものであるかを帰属することは,必ずしも容易ではない.不対電子を持つHO3やH2O-HO2の場合には,観測された吸収線が常磁性を示すこと,スピン分裂が存在すること,水素核による超微細分裂が存在することなどにより,分子の帰属ができる.また,高精度の分子軌道計算により構造を見積り,スペクトルを予測できる.これも分子種の同定の大きな手助けになる.また,本研究では,通常のマイクロ波分光法の他に,二つのマイクロ波あるいはミリ波を分子に同時に吸収させる2重共鳴分光法を用いた.これは,特に常磁性を示さない,HO3Hのスペクトルの帰属に重要な役割を果たした.
結 果
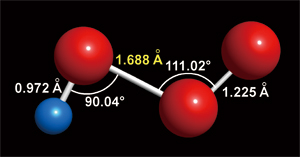 図2 HO3ラジカルの構造
図2 HO3ラジカルの構造スペクトルの解析の結果得られたそれぞれの分子の構造を図2−4に示す.マイクロ波分光の結果だけでは完全な構造パラメータを決めることができないので,上述の分子軌道計算の結果も援用した.ここでHO3とHO3Hはともに酸素原子が3つ直鎖状に結合した分子である.炭素や窒素の場合には長い直鎖状の結合が知られているが,酸素についてこのように3つの原子が直鎖になった分子が明確に気相で検出されたのは,我々の結果が最初である.しかし,それぞれの構造を見ると,その結合は二つの分子種でかなり異なっている.HO3Hの二つのO-O結合は長さが等しく,わずかにHOOHのそれより短い.即ちその結合は安定な単結合と解釈できる.これに対し,HO3の場合,OHとOOの間のO-O結合は結合距離が異常に長い.また,分子軌道計算からもこの結合は,水素結合のような分子間力と同程度の極めて弱いものであることが示された.これは,OH基をFやClに置き換えたFO2やClO2とも共通する構造的特徴である.この構造からこのラジカルの特徴を一言で記述すると,これはOHラジカルが酸素分子O2と弱い結合で会合したようなラジカルであるということになる.OHラジカルが大気化学で重要な分子種であり,大気中には20%の酸素分子が存在することを考えると,このラジカルが大気化学で重要な役割を果たすことは充分に考えられることである.実際,このラジカルの検出は大気化学の分野で広く注目を集めている.また,このラジカルの最安定構造は,図2のようなトランス型であると実験から結論されたが,これは多くの理論計算の予測に反した結果であった.HO3Hの構造も図のように二つの水素原子が互いに反対の方向につきだしたトランス型であると結論された.これはキラルな分子で,内部回転により右手系と左手系との間の反転分裂が可能であるが,その障壁は十分高く反転分裂は観測されていない.
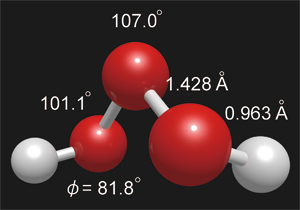 図3 HO3H分子の構造.キラルな分子で,これと鏡像対称な構造も存在する.
図3 HO3H分子の構造.キラルな分子で,これと鏡像対称な構造も存在する.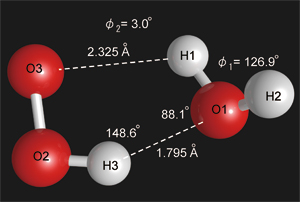 図4 ラジカル錯体H2O-HO2の構造.図のO1とH3の間には強い水素結合が存在.一方,H1とO3の間の結合は極めて弱く,H1とH2の役割の交換が可能である.
図4 ラジカル錯体H2O-HO2の構造.図のO1とH3の間には強い水素結合が存在.一方,H1とO3の間の結合は極めて弱く,H1とH2の役割の交換が可能である.これら二つの分子種と異なり H2O-HO2は,水分子とHO2ラジカルの錯体である.図の構造から明らかなことは,HO2の水素原子と水分子の酸素原子の間に水素結合があることである.その結合距離がかなり短いことから,その水素結合は通常のものに比べかなり強いものである.また,水の水素原子の一つはHO2の末端の酸素原子と弱い結合をしているが,その結合はかなり弱く,水分子は比較的容易に回転して結合している水素原子を入れ替える.スペクトルにはこの水素原子の交換によるスペクトルの分裂が観測されている.
まとめ
酸素分子が3個連なった構造を持つ二つの分子の気相のスペクトルを初めて観測し,その構造を精密に決定した.二つの分子の結合はかなり異なっており,HO3はOHラジカルと酸素分子の会合体とも云うべき構造を取っていることが明らかになった.この点でHO3は,H2O-HO2とともに大気化学で重要な役割を果たしていることが期待される分子種であるといえる.今回の結果を元に,今後,大気化学でのこれらの分子種の重要性を明らかにするような研究が進展することが大いに期待される.
HO3Hはまた,星間分子としても存在する可能性もある.我々の観測したスペクトルに対応する位置に,電波望遠鏡でスペクトル線が観測されている.そこで星間分子としての存在を確認するための電波望遠鏡での観測を進めている.現在までの所,観測が不十分で充分な確認に至っていないが,もしこのような分子が星間雲中に存在するとすると,星間雲での酸素の存在形態に全く新しい情報を与えると期待される.